In ons andere artikel hebben we actieve kool geïntroduceerd; de structuur, waarvan het is gemaakt, de belangrijkste vormen en hoe het wordt geproduceerd. In dit artikel leggen we uit hoe actieve kool werkt.
Koolstofadsorptie?
Let op: er is een belangrijk en duidelijk verschil tussen ADsorptie en ABsorptie:

Adsorptie wordt veroorzaakt door London-dispersiekrachten, een type van-der-waalskrachten of elektrostatische krachten die tussen alle moleculen bestaan. Van-der-waalskrachten zijn niet-specifiek en zijn relatief zwakke elektrische krachten die neutrale moleculen naar elkaar toetrekken in vloeistoffen, lucht en gassen.
London-dispersiekrachten zijn aantrekkingskrachten met een kort bereik en zijn daarom zeer gevoelig voor de afstand tussen het oppervlak van de actieve kool en het molecuul dat wordt geadsorbeerd. Deze krachten zijn echter additief.
Dit betekent dat de adsorptiekracht op de adsorptieplaats de som is van alle interacties tussen de koolstofatomen en het te adsorberen molecuul. Door het korte bereik en het additieve karakter van deze krachten wordt aangenomen dat actieve kool de sterkste fysieke adsorptiekrachten en het hoogste adsorptievolume heeft van alle bekende materialen.
Daarom treden de sterkste adsorptiekrachten op wanneer de afstand tussen de koolstofplaatjes en het te adsorberen molecuul zeer klein is, waardoor er sprake is van de sterkste adsorptie-energie.
Adsorptie is de afzetting van verbindingen (adsorbaten) uit water of een oplossing, of de condensatie van gassen op het oppervlak van de actieve kool (of het adsorbent). Deze adsorbaten ondergaan een faseverandering bij adsorptie omdat ze een veel lagere energie hebben zodra ze geadsorbeerd zijn. Adsorptie vindt daarom feitelijk plaats via energetische interacties en niet via een proces van moleculaire zeving.
Actieve kool zwelt echter niet op zoals een ionenwisselaarshars of een spons. Dit komt doordat al het werk diep in de koolstofstructuur gebeurt, waar het adsorberende molecuul eventuele watermoleculen op het interne oppervlak verdringt.
Verontreinigende moleculen worden effectief op hun plaats gehouden op het binnenste koolstofoppervlak en verwijderd dankzij de talrijke interacties in de koolstof-“porie”.
Structuur van actieve kool
Een bed van actieve kool bestaat uit ongeveer
- 40% bestaande uit de holtes tussen de koolstofdeeltjes; dit is het draineerbare volume als het koolstofbed zich in een oplossing bevindt.
- 20% wordt beschouwd als het volume van het koolstofdeeltje zelf, dat het koolstofskelet vormt.
- 40% wordt beschouwd als het totale ‘porievolume’ binnen het koolstofdeeltje, wat het niet-draineerbare volume is.
Als we vervolgens alleen kijken naar de individuele koolstofkorrel of het deeltje zelf, bestaat dit uit ongeveer: –
- 35% als het volume van het koolstofskelet,
- 25% als het ‘transportporie’-volume
- 40% als het ‘adsorptieporie’-volume
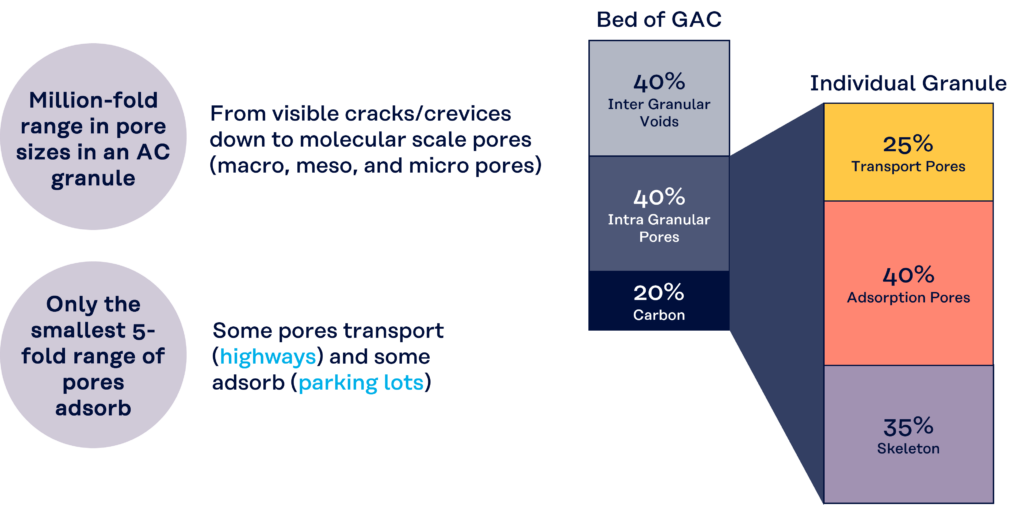
Het ‘transportporie’-volume bestaat uit grote poriën die in grootte variëren van de grootste van 0,1 micron tot zichtbare barsten en spleten in het deeltje van 0,1 mm.
Deze ‘transportporiën’ fungeren als een diffusiepad om de verontreiniging van buiten de koolstofstructuur naar het deeltje en naar de adsorptieplaats te transporteren. Ze bevatten concentratie- of drukgradiënten die het poriediffusieproces aandrijven en zo de verontreiniging naar de adsorptieplaatsen leiden.
Deze poriën zijn veel groter dan de grootste adsorptieporiën en zijn niet in staat om verontreinigingen te adsorberen, zelfs niet onder omstandigheden die de verzadiging benaderen. Daarom wordt elke oplossing in deze poriën als potentieel terugwinbaar beschouwd.
De onderstaande illustratie toont een adsorberende verbinding (adsorbaat) in een vloeistof die door het actieve koolbed, door het deeltje zelf en vervolgens naar de adsorptieplaats diffundeert.
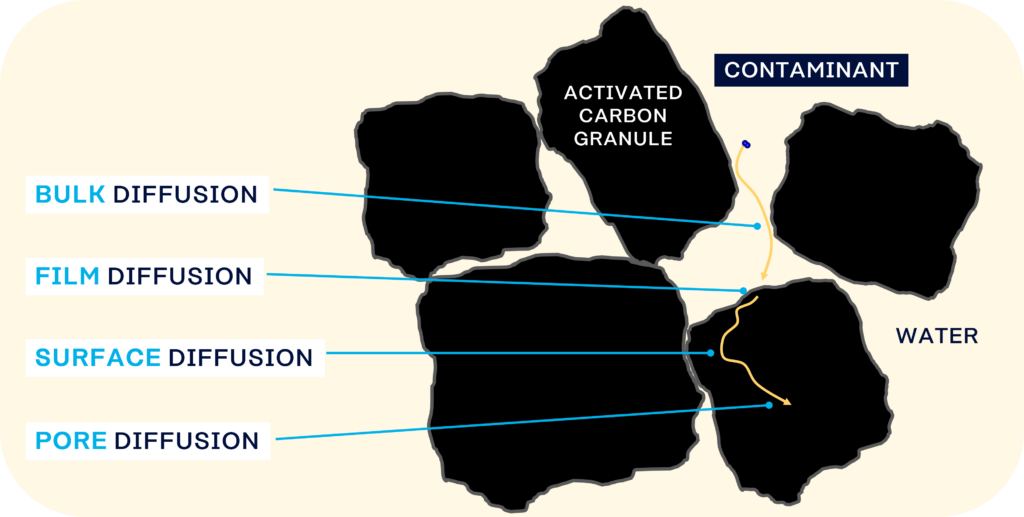
De ‘adsorptieporiën’ zijn de fijnste poriën in de koolstofstructuur en de delen van de koolstofstructuur die het adsorptievermogen hebben. Deze adsorptieporiën zijn de openingen, barsten en spleten tussen de grafietplaten waar voldoende intermoleculaire krachten aanwezig zijn om adsorptie te laten plaatsvinden. De breedtes van deze structuur hebben moleculaire afmetingen en zijn niet groter dan 10 tot 50 nm.
Adsorptie vindt alleen plaats in de adsorptieporiegebieden en bij verzadiging zijn alle adsorptieporiegebieden gevuld. Daarom wordt elke oplossing in deze poriën als niet-terugwinbaar beschouwd.
Het te adsorberen molecuul moet zich dicht bij een koolstofplaat bevinden om te kunnen adsorberen. Zodra het adsorbaat meer dan een paar moleculaire diameters van het koolstofoppervlak verwijderd is, vindt er geen adsorptie meer plaats.
Hoe werkt actieve kool?
Actieve kool werkt via een proces van adsorptie dankzij de poriestructuur, het grote oppervlak en de hoge oppervlaktereactiviteit.
De belangrijkste factoren die de adsorptie op actieve kool beïnvloeden zijn:
- Concentratie – de belading in gewichtsprocenten op de kool neemt toe naarmate de concentratie van de inkomende verontreiniging toeneemt.
- Structurele complexiteit – complexere structuren worden gemakkelijker geadsorbeerd
- Moleculair gewicht – hoe hoger het moleculair gewicht van de verontreiniging, hoe beter deze wordt geadsorbeerd
- Temperatuur – hoe hoger de temperatuur van het influent, hoe slechter de verontreiniging wordt geadsorbeerd.
In de vloeistoffase gaan de moleculen van de te verwijderen verbinding van de bulkvloeistof naar adsorptie in de poriën van de actieve kool, in een semi-vloeibare toestand. De extra factor die de adsorptie in de vloeistoffase beïnvloedt is
- Oplosbaarheid – hoe hoger de oplosbaarheid, hoe moeilijker het te adsorberen is
Daarom neemt de adsorbeerbaarheid van een organisch molecuul toe bij een toenemend moleculair gewicht en een afnemende oplosbaarheid.
De damp- of gasfase is een condensatieproces waarbij de adsorptiekrachten de moleculen van de verbinding condenseren tot een vloeistof. Deze kan vervolgens uit de lucht- of gasfase worden verwijderd binnen de poriën van de actieve kool. De extra factoren die de adsorptie in de dampfase beïnvloeden zijn:
- Dampspanning – verbindingen met een lagere dampspanning zijn beter adsorbeerbaar dan verbindingen met een hoge dampspanning.
- Relatieve vochtigheid – een lagere relatieve vochtigheid leidt tot een betere adsorptie
- Polariseerbaarheid – hoe hoger de polariteit, hoe moeilijker het te adsorberen is
De werkelijke levensduur van een koolstofbed is echter afhankelijk van vele andere factoren. Deze omvatten het geselecteerde type koolstof, de specifieke verontreiniging en concentratie die moet worden verwijderd, en vervolgens het vereiste behandelingsniveau voor de verontreiniging of verontreinigingen.
Daarnaast zijn de algemene toepassingsomstandigheden belangrijk. Deze omvatten welke andere verbindingen aanwezig kunnen zijn en hun concentraties, en het geïnstalleerde of geplande systeemontwerp inclusief de EBCT – empty bed contact time (contacttijd in een leeg bed).
Welke verbindingen kunnen op actieve kool worden geadsorbeerd?
Alle verbindingen zijn tot op zekere hoogte adsorbeerbaar op actieve kool. Verbindingen die gemakkelijk worden geadsorbeerd zijn aromatische en gechloreerde verbindingen, PFAS, VOS en kleurstoffen.
In de praktijk wordt actieve kool voornamelijk gebruikt voor de adsorptie van organische verbindingen en sommige anorganische verbindingen wanneer een geïmpregneerde actieve kool wordt gebruikt.
Afhankelijk van de toepassing kunnen verschillende soorten actieve kool nodig zijn. Het is belangrijk om de juiste kwaliteit en grootte te selecteren met betrekking tot de te verwijderen verontreiniging of de gewenste zuiverheidsgraad.
Bij Chemviron hebben we meer dan 80 jaar ervaring in het ontwerpen, produceren en implementeren van actieve kooloplossingen. In die tijd hebben we een bibliotheek opgebouwd met praktijkgegevens en prestatie-informatie.
Met behulp van deze gegevens en onze eigen modellen is Chemviron beter in staat om de waarschijnlijke prestaties van actieve kool te voorspellen. Wij kunnen daarom effectievere behandelingsoplossingen op maat maken op basis van het concept van adsorptie-energie, in plaats van de inmiddels verouderde definities van micro-, meso- en macroporiën.
Zie de volgende secties waar de specifieke te verwijderen verbindingen in meer detail worden behandeld.







